Tratamientos para la Esclerosis Múltiple
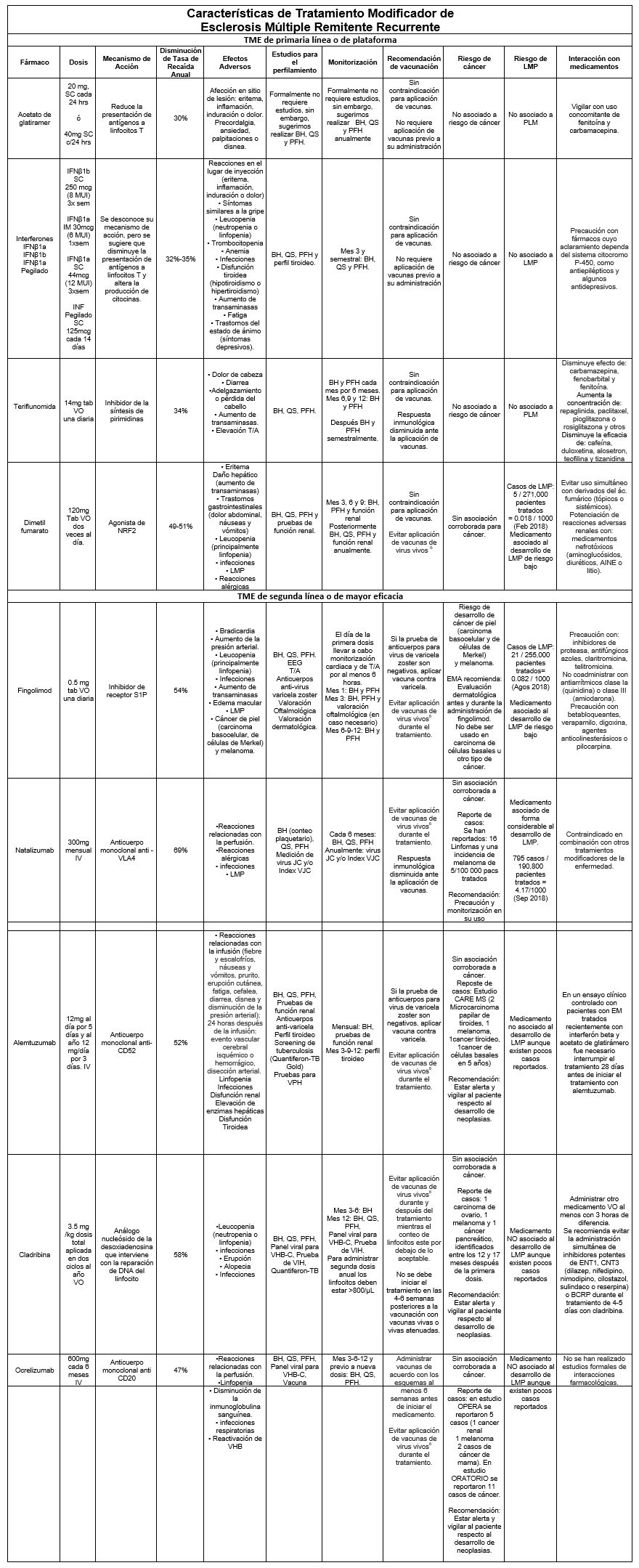
TME: tratamiento modificador de la enfermedad; LMP: Leucoencefalopatía multifocal progresiva; SC: subcutáneo, IM: intramuscular, IV: Intravenoso, VO: vía oral, BH: biometría hemática; QS: química sanguínea; VHB: virus de hepatitis B; VHC: virus de hepatitis C; PFH: pruebas de función hepática; EMA: European Medicines Agency; VPH: virus de papiloma humano.
Ejemplos de vacunas de virus vivos: (sarampión, paperas, rubéola, polio, rotavirus, tifoidea, fiebre amarilla, varicela, zóster y la vacuna nasal para la influenza).
Este cuadro es una guía para el médico, sin embargo, se recomienda revisar la ficha técnica de cada fármaco.
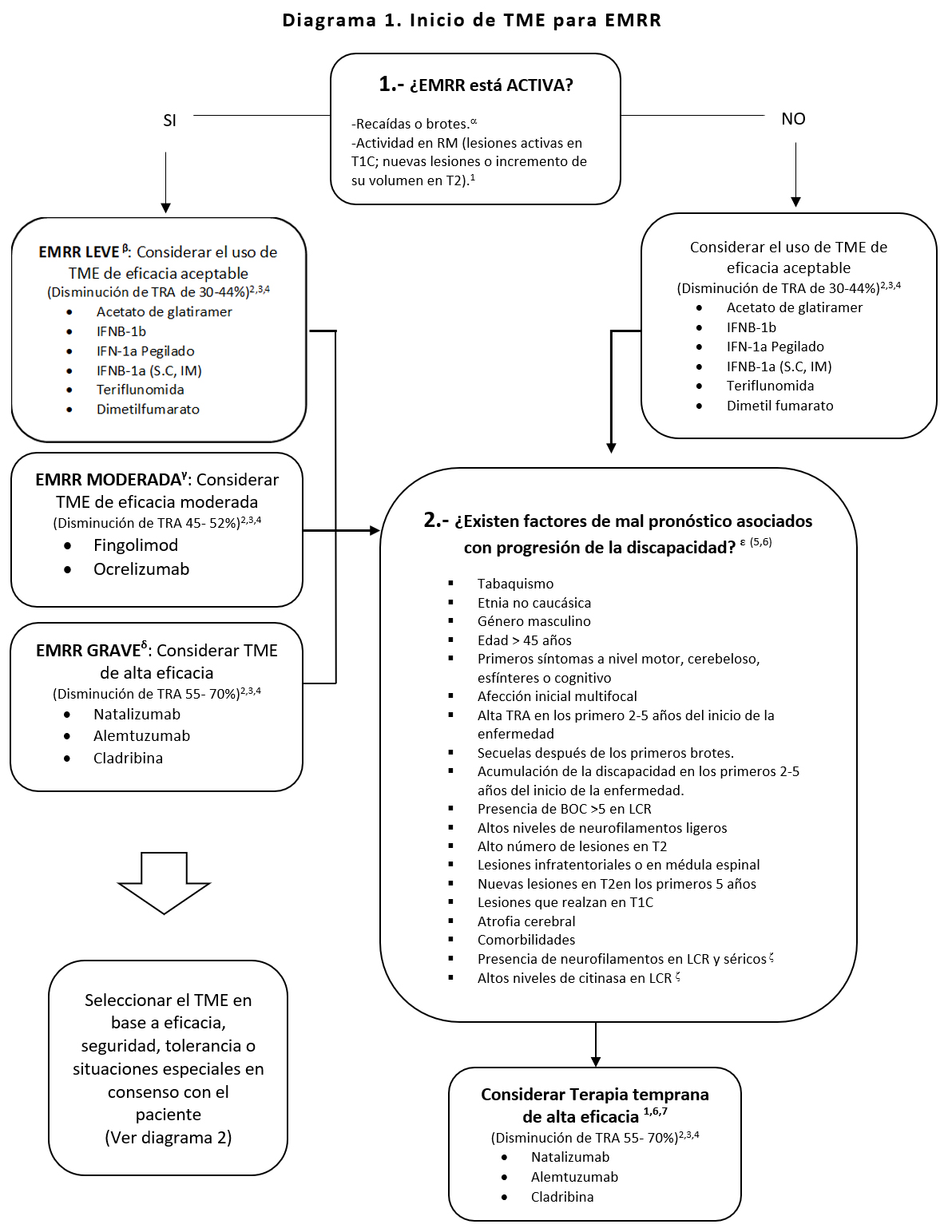
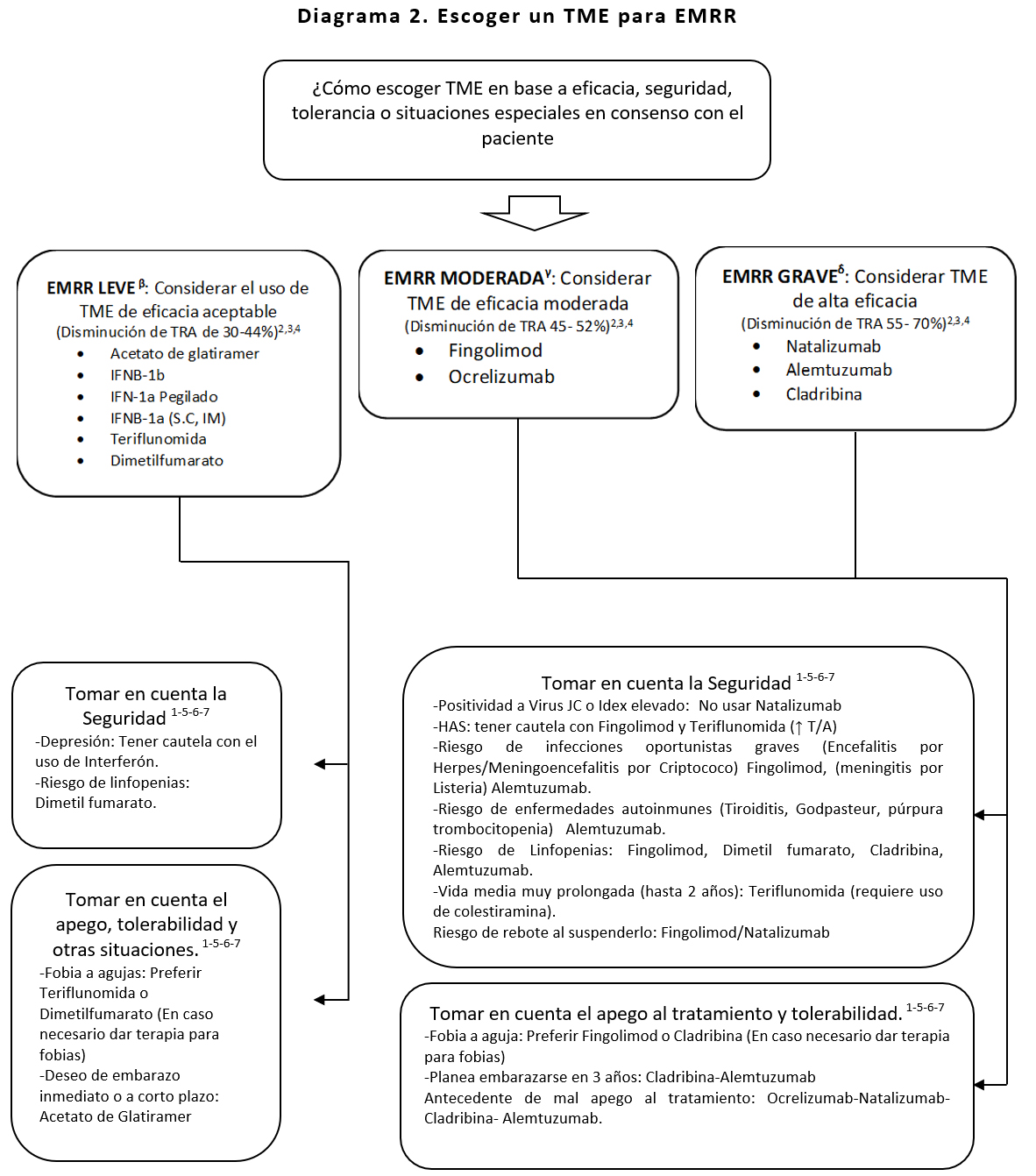
EMRR: Esclerosis Múltiple Remitente Recurrente; RM: Resonancia Magnética; TRA: Tasa de Recaída Anual; TME: Tratamiento Modificador de la Enfermedad; TRA: Tasa de Recaída Anual; BOC: Bandas Oligoclonales; LCR: Líquido Cefalorraquídeo; Virus JC: virus John Cunningham; T/A: Tensión Arterial.
En las guías aún no sé menciona la definición clínica de recaídas, pero se ha mencionado en la literatura las siguientes definiciones: >1 recaída en los últimos 6 meses / > de 2 recaídas en los últimos 6 meses.
La definición de EMRR leve recientemente se ha tratado de homogenizar con el término “benigna”, que consiste en baja progresión de la discapacidad (<3 puntos de EDSS) después de 10-15 años de evolución y/o baja frecuencia o ausencia de brotes sin generación de discapacidad. 8,9 En una publicación reciente, la definición de EMRR leve está basada en el incumplimiento de NEDA 1 y 2 (Sin brotes o recaídas/ Sin actividad en MRI (lesions nuevas o aumento de volumen de lesions en T2).6
No hay una definición consensuada de EMRR moderada en las guías de EMRR, sin embargo, se ha propuesto que se defina como el incumplimiento de NEDA 1,2 y3 (Sin brotes o recaidas /Sin actividad en MRI (lesions nuevas o aumento de volumen de lesions en T2 / Progresión de discapacidad confirmada). 6
Se diagnostica EMRR grave, agresiva o de gran actividad, cuando tiene uno o más de los siguientes criterios: 1) EDSS de 4 puntos en los primeros 5 años del inicio de la enfermedad. 2) Dos o más ataques clínicos con resolución incompleta dentro de un año. 3) Dos o más estudios de RM con nuevas lesiones activas (captan contraste) o incremento en el tamaño de las lesiones en T2, a pesar de tratamiento. 4) Sin respuesta terapéutica con el uso de uno o más TME durante más de un año. 10
Los factores de riesgo mencionados han demostrado ser predictores de la progresión de la discapacidad, sin embargo, consideramos que no todos cuentan con la misma trascendencia para tomar la decisión de escoger el TME, pero no se encuentra establecida en la literatura esta diferencia de factores de riesgo de progresión alto (por ejem; alta TRA, acumulación de la discapacidad, alto número de lesiones en T2, lesiones que realzan en T1C, etc,), o riesgo de progresión bajo (género masculino, niveles séricos de vitamina D, etnia no caucásica).
Factores de riesgo de progresión de discapacidad corroborados, pero no disponibles en México, solo en el extranjero.
Referencias
Aquellos pacientes que tiene diagnóstico de Esclerosis Múltiple Remitente Recurrente después de 15 a 20 años de evolución tienen riesgo de que la enfermedad se convierta a Esclerosis Múltiple Secundariamente Progresiva (EMSP). Este tipo de Esclerosis tiene un mayor potencial degenerativo y se caracteriza por la disminución en la aparición de brotes, acompañado de un mayor deterioro en diferentes funciones neurológicas y acumulación de la discapacidad. (1)
Recientemente se han aprobado tres medicamentos para tratar la “Esclerosis Múltiple Secundaria Progresiva activa”; aunque la definición de este término no se encuentra en las diferentes guías y artículos de Esclerosis Múltiple, el término aislado “activa” se refiere a la presencia de Brotes o recaídas y/o incremento en el número de lesiones o su volumen en secuencias T2 y/o lesiones que realzan con medio de contraste en secuencia T1C. (2)
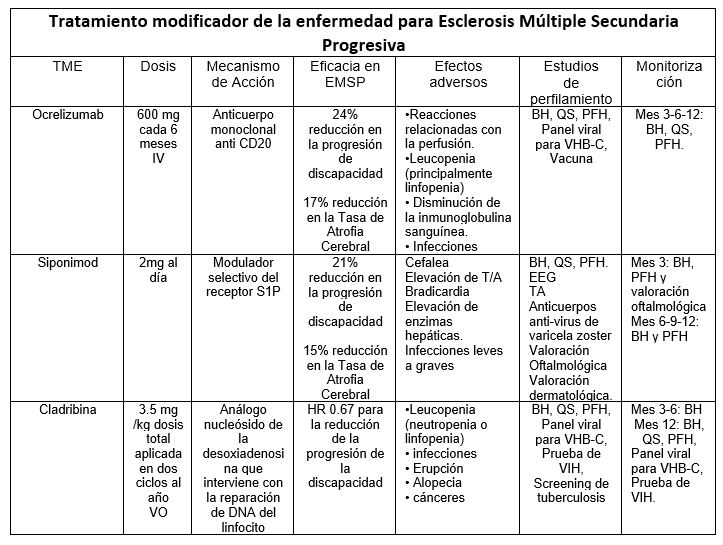
La situación de los TME para la EMSP ante las diferentes instancias de farmacovigilancia a nivel mundial es la siguiente (1):
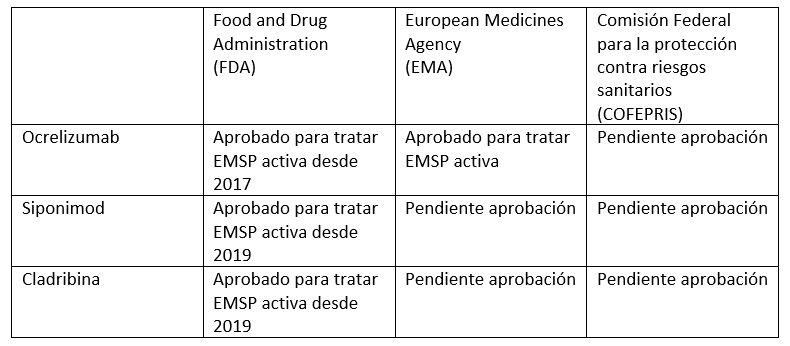
Ocrelizumab
Es un anticuerpo monoclonal humanizado anti CD20, cuyo resultado es la depleción de célula B y la producción de anticuerpos. Ocrelizumab, a través del estudio ORATORIO realizado en pacientes con formas progresivas de la enfermedad, demostró reducir el riesgo de progresión de la discapacidad en un 24% después de 12 semanas y disminuir la tasa de atrofia cerebral en un 17.5%. (3)
Siponimod
Es un modulador selectivo del receptor S1P, específicamente de la subunidad 5. En el estudio EXPAND hecho en pacientes con EMSP, la administración de Siponimod disminuyó el riesgo de progresión de discapacidad confirmada en un 21% comparado con placebo a los 3 meses y 26% a los 6 meses. (4)
Cladribina
Es un nucleósido de purina fosforilado a nivel intracelular cuyo efecto es la muerte celular de linfocitos en una primera fase, para después alcanzar un efecto de inmuno-reconstitución. El estudio CLARITY realizado en pacientes con EMRR evidenció una disminución del riesgo de progresión de discapacidad a tres meses. En otro estudio llamada ONWARD, dirigido a pacientes con EM progresivas para comparar la eficacia de cladribina contra INF-β y placebo, se observó una reducción del riesgo de acumulación de progresión de discapacidad por arrojar un HR de 0.67. (5)
Referencias
